
清空記錄
歷史記錄
取消
清空記錄
歷史記錄



樂(lè)朗小課堂 | 已上市生物制品包裝材料和容器變更和技術(shù)要求(二)——制劑
包材生產(chǎn)工藝變更、質(zhì)量標(biāo)準(zhǔn)變更等可能對(duì)已上市生物制品質(zhì)量產(chǎn)生影響,進(jìn)而對(duì)其產(chǎn)生影響的變更,包材登記人及生物制品持有人應(yīng)按《國(guó)家藥監(jiān)局關(guān)于進(jìn)一步完善藥品關(guān)聯(lián)審評(píng)審批和監(jiān)管工作有關(guān)事宜的公告》(2019年第56號(hào))規(guī)定進(jìn)行變更研究及變更管理。
按藥學(xué)變更可能對(duì)生物品安全性、有效性和質(zhì)量可控性的風(fēng)險(xiǎn)和產(chǎn)生影響的程度,實(shí)行變更分類。依據(jù)風(fēng)險(xiǎn)和產(chǎn)生影響的程度由高到低分為:重大變更、中等變更、微小變更。
依據(jù)國(guó)家藥監(jiān)局藥審中心關(guān)于發(fā)布《已上市生物制品藥學(xué)變更研究技術(shù)指導(dǎo)原則(試行)》的通告(2021年第31號(hào)),生物制品-制劑常見(jiàn)變更類別及技術(shù)要求如下:
(二)制劑 (3.2.P)
A、規(guī)格C、生產(chǎn)場(chǎng)地、規(guī)模和工藝

備注:*前提條件與技術(shù)要求詳見(jiàn)《已上市生物制品藥學(xué)變更研究技術(shù)指導(dǎo)原則(試行)》的通告(2021年第31號(hào))五、生物制品常見(jiàn)變更類別及技術(shù)要求-(二)制劑 (3.2.P) A、規(guī)格。
C、生產(chǎn)場(chǎng)地、規(guī)模和工藝

備注:*前提條件與技術(shù)要求詳見(jiàn)《已上市生物制品藥學(xué)變更研究技術(shù)指導(dǎo)原則(試行)》的通告(2021年第31號(hào))五、生物制品常見(jiàn)變更類別及技術(shù)要求-(二)制劑 (3.2.P) C、生產(chǎn)場(chǎng)地、規(guī)模和工藝。
G、包裝系統(tǒng)
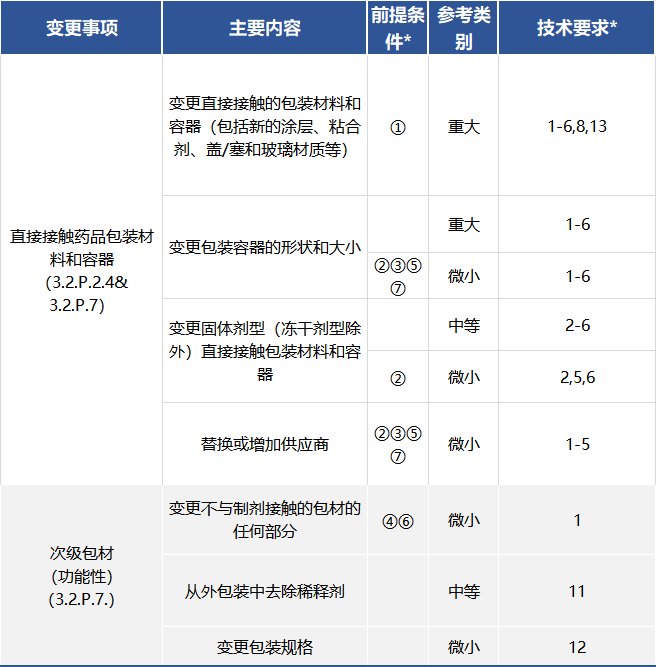
備注:*前提條件與技術(shù)要求詳見(jiàn)《已上市生物制品藥學(xué)變更研究技術(shù)指導(dǎo)原則(試行)》的通告(2021年第31號(hào))五、生物制品常見(jiàn)變更類別及技術(shù)要求-(二)制劑 (3.2.P) G、包裝系統(tǒng)。
原文下載鏈接:
https://www.cde.org.cn/main/news/viewInfoCommon/7ef3a0d630aea8a49186f49f31a6fd3c
Lelangtek可提供相關(guān)服務(wù),歡迎致電交流
咨詢電話:400-008-6228

 簡(jiǎn)體中文
簡(jiǎn)體中文
 瀏覽器自帶分享功能也很好用哦~
瀏覽器自帶分享功能也很好用哦~







